Cardiovascular Pathology
14
Produits
Abdominal Aortic Aneurysm
Histoire clinique Un homme de 70 ans avec un reflux gastro-œsophagien léger a présenté une douleur abdominale haute sévère soudaine irradiant vers l’épaule gauche. À l’examen, il était en détresse et hyperventilait, pouls 87/min, tension artérielle 140/90 mmHg. L’examen abdominal révélait une rigidité en planche et une diminution des bruits intestinaux. La laparotomie d’urgence n’a pas montré de viscère rompu ; le pancréas était normal, mais un anévrisme abdominal non rompu a été noté. L’endoscopie du lendemain a révélé un ulcère œsophagien rompu, et une sonde de Celestin a été posée. Malgré le traitement, le patient a développé des complications infectieuses locales, un œdème pulmonaire, une congestion, et est décédé 19 jours après l’admission.Pathologie Le spécimen comprend le segment inférieur de l’aorte abdominale avec les vaisseaux iliaques communs et les portions proximales des artères iliaques internes et externes. Un large anévrisme de 10 x 7 cm se situe sous l’origine des artères rénales, s’étendant jusqu’à la bifurcation aortique. La paroi de l’anévrisme est très amincie et partiellement tapissée d’un thrombus laminé, signe de chronicité. Un thrombus récent est aussi visible. Une dilatation anévrismale des artères iliaques communes et de l’artère iliaque externe gauche est présente. La partie supérieure de l’aorte montre plusieurs plaques athéromateuses ulcérées localement. Aucune rupture n’a été observée. Informations complémentaires Un anévrisme de l’aorte abdominale (AAA) est une dilatation localisée de l’aorte abdominale (diamètre >3 cm ou plus de 50 % supérieur à la normale). La plupart des AAA sont asymptomatiques sauf en cas de rupture. Les gros anévrismes peuvent être palpables, parfois une douleur abdominale, dorsale ou aux jambes survient. La rupture provoque une douleur soudaine, une hypotension, une perte de conscience et souvent la mort. Les AAA touchent surtout les hommes de plus de 50 ans, en particulier les fumeurs ou les personnes hypertendues ou ayant des antécédents familiaux. Des maladies génétiques comme le syndrome de Marfan ou d’Ehlers-Danlos augmentent aussi le risque. Environ 85 % des AAA se situent sous les reins, ce qui en fait la forme la plus fréquente d’anévrisme aortique.
Tetralogy of Fallot
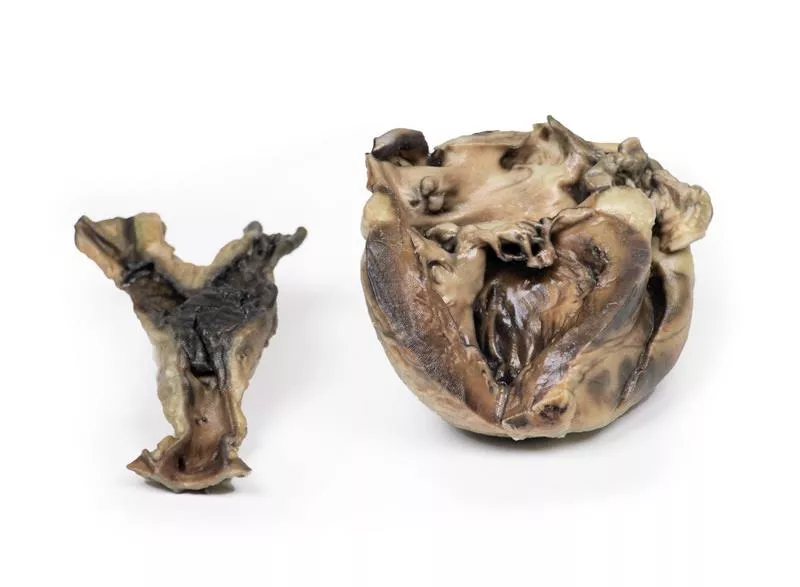
Histoire cliniqueUn garçon de 21 mois a été hospitalisé pour dyspnée à l’effort et épuisement évoluant depuis 2 à 3 mois. Plusieurs épisodes de dyspnée aiguë de courte durée avaient été rapportés. À l’examen, il présentait une cyanose centrale, un hippocratisme digital léger et un souffle systolique rude au bord gauche du sternum. Le cathétérisme a confirmé une Tétralogie de Fallot avec œdème pulmonaire sévère. Une anastomose Willis-Potts a été réalisée. L’enfant est malheureusement décédé 12 heures après l’intervention suite à une dyspnée aiguë et une consolidation du lobe gauche.Pathologie Vue de face, la pièce cardiaque montre une hypertrophie du ventricule droit avec rétrécissement de la voie d’éjection pulmonaire. La valve pulmonaire est bicuspide et sténosée, avec fibrose endocardique sous-jacente. La aorte surplombe un large défaut septal ventriculaire (VSD) et communique avec le ventricule droit. Une sonde peut être introduite depuis le tronc pulmonaire rétréci dans l’artère pulmonaire gauche dilatée et à travers l’anastomose chirurgicale vers l’aorte descendante. L’arrière du cœur révèle deux défauts septaux auriculaires (ASD). La paroi du ventricule gauche est plus mince que celle du droit. Informations complémentairesLa Tétralogie de Fallot comporte quatre malformations : 1. Défaut du septum ventriculaire, 2. Aorte chevauchant le VSD, 3. Sténose pulmonaire, et 4. Hypertrophie du ventricule droit. La cyanose apparaît tôt et dépend de la sévérité de l’obstruction pulmonaire. Certains patients survivent sans traitement jusqu’à l’âge adulte, mais la chirurgie corrective est aujourd’hui la norme. D’autres anomalies comme un ASD peuvent être présentes. Des causes génétiques incluent la trisomie 21 et le syndrome de DiGeorge.
Atrial septal defect
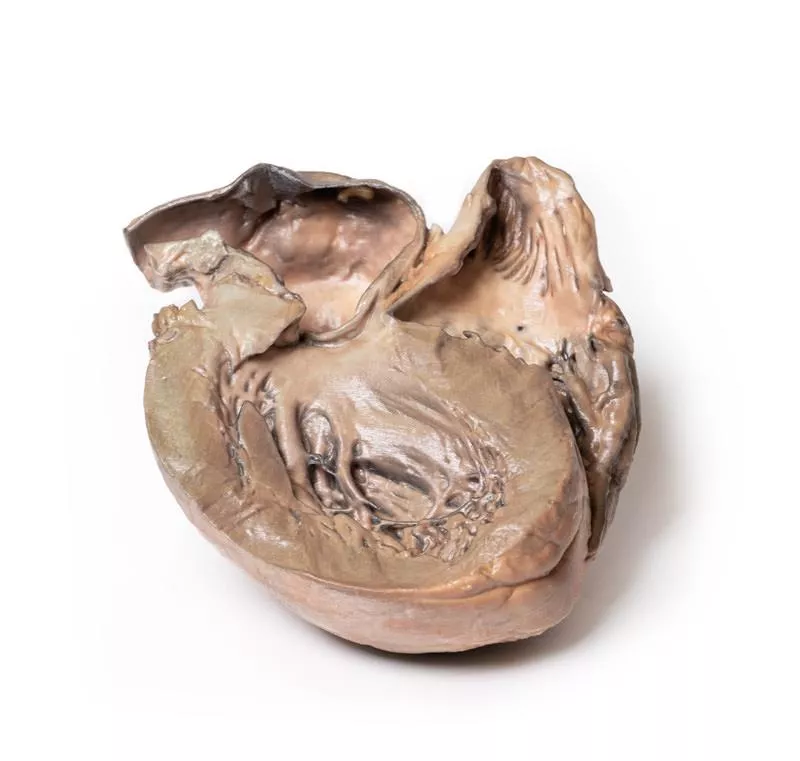
Histoire clinique Une fille de 10 ans avec une cardiopathie congénitale connue a été hospitalisée pour réparation chirurgicale en raison d’une apparition récente de cyanose et d’insuffisance cardiaque. Elle était essoufflée, avec une tension artérielle de 105/60 mmHg et un pouls de 140/min. L’examen montrait un souffle cardiaque fort au 4e espace intercostal gauche près du sternum, une pression veineuse jugulaire élevée et des râles basaux bilatéraux sans œdèmes périphériques. La réparation fut réalisée, mais la patiente est décédée suite à une détérioration post-opératoire brutale d’origine inconnue.Pathologie Le cœur vu de gauche présentait une large fente ovale de 3,5 cm dans le septum interauriculaire, avec seulement un mince bord postéro-inférieur résiduel. Le ventricule gauche était petit, le ventricule droit hypertrophié, visible par la paroi postéro-latérale épaissie. L’artère pulmonaire était fortement dilatée, avec l’arc aortique au-dessus et l’auricule gauche à proximité. Informations complémentairesLe défaut du septum atrial (DSA) est souvent asymptomatique dans la petite enfance, même s’il est important. Les symptômes apparaissent plus tard avec l’inversion du shunt gauche-droite causée par l’hypertrophie ventriculaire droite et l’hypertension pulmonaire, entraînant un shunt droite-gauche, cyanose, dyspnée et insuffisance cardiaque. Types de DSA : - Secundum : Le plus courant, au centre du septum atrial. - Primum : Partie inférieure du septum, souvent associé à d’autres malformations. - Sinus venosus : Rare, partie supérieure, fréquemment associé à d’autres anomalies. - Sinus coronaire : Rare, absence de la paroi entre sinus coronaire et oreillette gauche.La cause exacte est inconnue. Certains défauts sont familiaux ou liés à des conditions génétiques comme la trisomie 21. Les risques pendant la grossesse comprennent infections (ex : rubéole), usage de substances (drogues, tabac, alcool), exposition à des toxines et maladies maternelles telles que diabète ou lupus.
Bicuspid Aortic Valve
Histoire clinique Une femme de 64 ans se présente avec des douleurs thoraciques depuis 5 mois, accompagnées d’essoufflement et de sifflements expiratoires depuis 4 mois. À l’examen, elle était dyspnéique avec un sifflement expiratoire, des crépitements à gauche et des signes d’épanchement pleural droit. Le pouls et la tension étaient normaux. Un souffle systolique précordial et un battement d’apex intense étaient notés au 5e espace intercostal gauche. Aucun œdème périphérique n’était présent. La patiente est décédée 4 jours après son admission.Pathologie Le cœur a été ouvert pour exposer le ventricule gauche et les valves. La valve aortique était bicuspide au lieu de tricuspide, avec un épaississement par endroits mais globalement normale. Les artères coronaires, y compris la circonflexe gauche, étaient bien ouvertes. Une fibrose péricardique dense et des adhérences sur la face postérieure du cœur témoignaient d’une péricardite constrictive. L’autopsie a aussi révélé une ascite, un foie cirrhotique atrophié, des épanchements pleuraux bilatéraux et un collapsus pulmonaire droit. La cause du décès était une cirrhose hépatique et une insuffisance hépatique, probablement liées à la péricardite. La valve aortique bicuspide était une découverte fortuite. Informations complémentaires La valve aortique bicuspide est une anomalie congénitale fréquente souvent asymptomatique jusqu’à l’âge adulte. Elle favorise la sténose aortique calcifiée, généralement entre la 5e et la 7e décennie. Elle peut être isolée ou associée à des syndromes comme la tétralogie de Fallot. La fusion de deux cuspides entraîne une taille inégale des feuillets, provoquant un mouvement anormal et des turbulences, ce qui augmente les risques de dilatation, dissection et calcification aortiques. Avec l’âge, une sténose ou une régurgitation aortique peut survenir, entraînant dyspnée et baisse de la tolérance à l’effort. Le diagnostic est confirmé par échocardiographie transthoracique.
Acute Bacterial Endocarditis
Histoire clinique Un garçon de 15 ans a présenté toux avec expectoration, puis une fièvre intermittente et des douleurs thoraciques quelques jours avant une admission en état de coma. L’examen a révélé un souffle diastolique précoce dans la zone aortique irradiant le long du bord gauche du sternum. Malgré un traitement antibiotique, son état s’est rapidement dégradé et il est décédé. Les hémocultures ont isolé Staphylococcus aureus.Pathologie Le petit cœur montre le ventricule gauche et les valves associées. Le cusp non coronaire de la valve aortique est ulcéré, perforé et porte des végétations friables. Une perforation s’étend sous ce cusp dans l’oreillette droite, au-dessus de la valve tricuspide. Un autre cusp aortique est épaissi. Il s’agit d’une endocardite bactérienne aiguë avec perforations des cuspides aortiques et atrioventriculaires. Informations complémentaires L’endocardite bactérienne aiguë est une infection sévère des valves cardiaques ou de l’endocarde, nécessitant souvent une lésion endothéliale préalable. Staphylococcus aureus est très virulent et peut infecter des valves normales. L’infection provoque l’agrégation de plaquettes et de fibrine formant des végétations qui se développent par activation de la coagulation et inflammation. Ces végétations peuvent emboliser et propager l’infection à distance. Les facteurs de risque incluent les maladies valvulaires (rhumatismales, congénitales), valves prothétiques ou interventions cardiaques antérieures. Le diagnostic repose sur l’examen clinique, les hémocultures et l’échocardiographie (transthoracique et transœsophagienne). Le traitement associe antibiotiques, anticoagulants et parfois chirurgie.
Syphilitic Aneurysm
Histoire clinique Un homme de 61 ans se présente avec une douleur thoracique angineuse à l’effort et une dyspnée, évoluant depuis 6 ans. À l’examen, il est cyanotique, tachycarde avec un pouls bondissant. Une tuméfaction et un souffle ont été notés sur le côté droit du cou. Le choc apex est déplacé en bas et en dehors. Un souffle systolique et diastolique intense est entendu dans la région aortique. La radiographie thoracique montre une cardiomégalie et une large masse arrondie dans le médiastin supérieur droit, continue avec l’ombre cardiaque, ainsi que des signes d’insuffisance cardiaque. Les tests sanguins sont positifs pour les anticorps anti-tréponémiques. Malgré le traitement, l’état du patient s’est aggravé et il est décédé d’une insuffisance cardiaque.Pathologie Le spécimen comprend le cœur hypertrophié, l’arc aortique et l’aorte descendante. L’aorte ascendante est dilatée jusqu’à 7 cm et présente une large bulle anévrismale de 11 x 13 cm. L’anévrisme a été ouvert, montrant une surface intime ridée et cicatricielle avec une athérome marquée. Les artères innominée, carotide commune gauche et sous-clavière sont déplacées vers la gauche par l’anévrisme. Une épaississement en forme de crête de 5 mm marque l’attache du péricarde. La congestion des petits vaisseaux dans l’adventice est marquée. Il s’agit d’un anévrisme syphilitique de l’arc aortique. Informations complémentaires La syphilis est une infection chronique causée par le spirochète Treponema pallidum, principalement transmise sexuellement, parfois congénitale. Les groupes à risque incluent les personnes sexuellement actives, les toxicomanes, les patients VIH et les hommes ayant des rapports sexuels avec des hommes. La pénicilline reste le traitement principal. La syphilis évolue en trois stades : - Syphilis primaire : environ 3 semaines après l’infection, avec un chancre indolore qui guérit spontanément. - Syphilis secondaire : provoque des symptômes généraux et des éruptions cutanées caractéristiques. - Syphilis tertiaire : survient après des années, avec atteinte cardiovasculaire, neurosyphilis et gummas.La syphilis cardiovasculaire implique une aortite de l’aorte ascendante, provoquant dilatation, insuffisance valvulaire et formation d’anévrismes par endartérite des vasa vasorum. Les symptômes apparaissent généralement 15 à 30 ans après l’infection. La neurosyphilis cause maux de tête, perte de vision, AVC et troubles cognitifs. La syphilis gummateuse se caractérise par des lésions nodulaires dans la peau, les os et les muqueuses, surtout chez les patients VIH.
Right Ventricular Hypertrophy
Histoire clinique Une femme de 56 ans atteinte d’emphysème présentait depuis deux ans une dyspnée d’effort progressive associée à des bronchites récidivantes. À l’examen, sa tension artérielle était de 160/90 mmHg, le pouls de 96/min, et la pression veineuse jugulaire augmentée de 6 cm. Le choc de pointe était impalpable, des râles crépitants bilatéraux étaient présents, ainsi qu’un œdème périphérique à godet. L’ECG montrait un signe de surcharge du cœur droit, et les gaz du sang indiquaient une acidose respiratoire. Malgré le traitement, la patiente s’est progressivement détériorée et est décédée.Pathologie Le cœur, vu de face, présentait un ventricule droit fortement hypertrophié et dilaté. Par ailleurs, le cœur semblait normal. Ceci est un cas d’hypertrophie ventriculaire droite (HVD) chez une patiente atteinte d’emphysème. Informations complémentaires L’HVD est souvent causée par des maladies pulmonaires chroniques ou des malformations cardiaques. Une cause principale est l’hypertension pulmonaire (HP), qui élève la pression dans l’artère pulmonaire, poussant le ventricule droit à s’hypertrophier. L’HP touche environ 4 personnes par million dans le monde, avec HVD dans environ 30 % des cas. Les causes fréquentes incluent la BPCO, l’embolie pulmonaire et d’autres maladies pulmonaires restrictives. L’HVD peut aussi résulter de malformations cardiaques telles que l’insuffisance tricuspide, la tétralogie de Fallot, les communications interventriculaires, la sténose de la valve pulmonaire et les défauts du septum atrial. L’HVD est également associée à l’obésité abdominale et à une pression artérielle systolique élevée.
Congenital Pulmonary Stenosis
Histoire clinique Ce garçon présentait un souffle cardiaque détecté à la naissance. Il est resté asymptomatique jusqu'à l'âge de 10 mois. Deux semaines avant son hospitalisation, il est devenu apathique, a développé une toux légère et a pris rapidement du poids. Dix jours avant l’admission, des œdèmes aux mains, aux pieds et au visage sont apparus. À l’examen, il était potelé, avec une tension artérielle de 90/59 mmHg. Un frémissement fin était palpable sur toute la région précordiale, avec un souffle systolique rude maximal au foyer pulmonaire. L’enfant est décédé malgré le traitement, des suites d’une insuffisance cardiaque congestive.Pathologie Le cœur de l’enfant, vu de gauche, montre une artère pulmonaire ouverte révélant une valve pulmonaire anormale. Elle forme un diaphragme conique épaissi avec une ouverture centrale de 2 mm. Une importante dilatation post-sténotique de l’artère pulmonaire est visible. Le cœur droit est dilaté, avec hypertrophie ventriculaire droite et dilatation de l’oreillette droite. Il s’agit d’une sténose isolée de la valve pulmonaire. Informations complémentaires La sténose pulmonaire représente environ 7?% des cardiopathies congénitales. Elle peut être isolée ou faire partie d’une malformation complexe comme la tétralogie de Fallot. Elle peut être légère, modérée ou sévère. Les formes sévères provoquent une hypertrophie du ventricule droit et peuvent évoluer vers une insuffisance cardiaque. Les complications incluent endocardite infectieuse et troubles du rythme. Le diagnostic repose sur l’échocardiographie, parfois complétée par l’IRM ou le scanner. Le traitement chirurgical est aujourd’hui bien établi.
Hydatid Disease Affecting the Heart and Aorta
Histoire cliniqueUne fille de 11 ans souffrait d’une hydatidose depuis 18 mois, ayant subi trois craniotomies pour retirer 17 kystes cérébraux. D’autres kystes ont été détectés aux reins, au mésentère et à la bifurcation de l’aorte abdominale. Une radio du cœur a révélé un kyste calcifié. Lors de son ablation, l’état s’est aggravé et la patiente est décédée. Un kyste hydatique mort a été retrouvé dans le ventricule gauche.Pathologie Le cœur ouvert dévoile une hypertrophie ventriculaire gauche et un canal anormal passant par la cuspide postérieure de la valve mitrale vers l’oreillette gauche, entouré de tissu fibreux avec des sutures visibles. L’aorte abdominale à la bifurcation iliaque contient un gros caillot anté-mortem. Des kystes hydatiques se trouvent dans la paroi aortique et le canal ventricule-oreillette, montrant les couches typiques avec kystes filles et réaction granulomateuse. Informations complémentairesLa maladie hydatique est causée par le ténia Echinococcus granulosus, transmis via les excréments de chien. L'ingestion d'œufs humains provoque des kystes, principalement dans le foie et les poumons. Bien que rares (0,5 à 2?%), les atteintes cardiaques peuvent être mortelles, avec un risque de tamponnade péricardique en cas de rupture.
Hypertrophic Subaortic stenosis
Histoire cliniqueUn touriste américain de 42 ans a été retrouvé mort dans sa chambre d'hôtel. Une autopsie médico-légale a été réalisée pour déterminer la cause du décès.Pathologie La coupe longitudinale du cœur montre les deux ventricules et le septum interventriculaire. On observe une hypertrophie marquée du septum et du ventricule gauche. Les valves aortique et mitrale semblent normales. L'épaississement du septum rétrécit la lumière du ventricule gauche.DiagnosticSténose sous-aortique hypertrophique idiopathique, également appelée cardiomyopathie hypertrophique. Informations complémentairesLa sténose sous-aortique est généralement acquise et résulte d’une anomalie structurelle du tractus d’éjection du ventricule gauche (LVOT). Cette anomalie provoque un flux sanguin turbulent, entraînant fibrose et épaississement progressifs. La conséquence est une hypertrophie du ventricule gauche due à l’augmentation de la pression aortique. Si la sténose est légère ou modérée, elle peut rester asymptomatique. Des symptômes comme la dyspnée à l’effort ou les syncopes peuvent apparaître lorsque la maladie progresse. Un souffle systolique à l’auscultation oriente le diagnostic, confirmé par échocardiographie. Le traitement définitif repose sur une correction chirurgicale de l’obstruction.
Rheumatic endocarditis
Histoire cliniqueUne femme de 52 ans a présenté une dyspnée progressive. Elle avait des antécédents de fièvre avec arthralgies migratrices dans l’enfance suite à un mal de gorge. À l’examen, elle était cyanosée, en fibrillation auriculaire, avec une hypertension veineuse jugulaire, un souffle pansystolique au niveau de l’apex, une hépatomégalie et un œdème. Elle a reçu de la digoxine, du furosémide et de la pénicilline, mais est décédée d’un arrêt cardiaque.Pathologie Le cœur ouvert montre l’oreillette et le ventricule gauches. La valve mitrale est épaissie. La paroi de l’oreillette gauche est recouverte de sang et de fibrine, et l’auricule contenant un caillot dû à la fibrillation auriculaire. Un thrombus mural et des épaississements endocardiques irréguliers – appelés plaques de MacCallum – sont présents à leur emplacement typique. Informations complémentairesCes signes sont très évocateurs d’une rhumatisme articulaire aigu, réaction auto-immune à une infection streptococcique non traitée. Elle peut affecter le cœur, les articulations, la peau et le cerveau. Les atteintes cardiaques répétées entraînent une cardiopathie rhumatismale chronique, souvent avec sténose mitrale due à une fibrose. On observe des nœuds d’Aschoff. Avec le temps, l’oreillette gauche se dilate, menant à une fibrillation auriculaire, à des thrombus muraux et finalement à une insuffisance cardiaque sévère.
Traumatic Oesophageal-aortic fistula
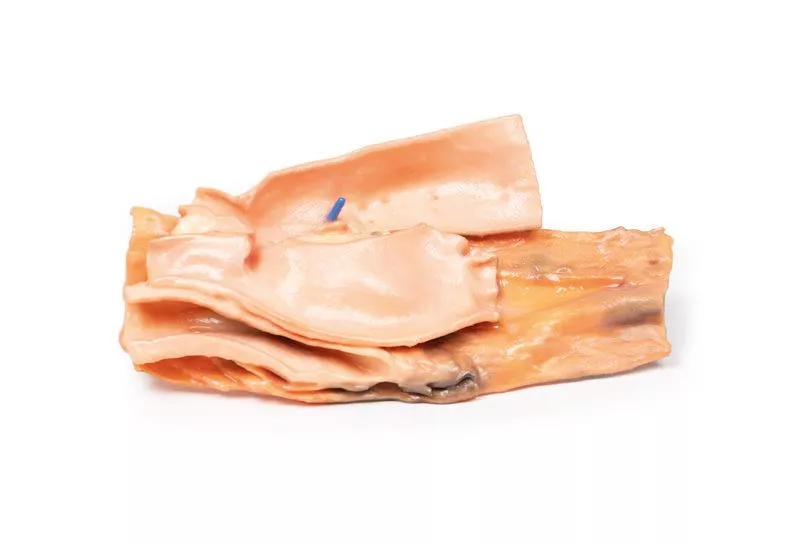
Histoire clinique Une femme a avalé un os de chop durant le déjeuner, puis s’est effondrée l’après-midi avec une hématémèse massive. Lors de la laparotomie, l’estomac était rempli de sang frais, sans cause identifiée. Elle est décédée le lendemain. L’autopsie a révélé une communication entre l’aorte et l’œsophage.Pathologie Le spécimen comprend la trachée distale, l’arc aortique (ouvert en plan coronal, vue antérieure) et l’œsophage (ouvert longitudinalement). La muqueuse œsophagienne est ulcérée et hémorragique. Une petite sonde montre une fistule entre l’œsophage et la paroi postérieure de l’aorte thoracique descendante. Informations complémentaires Bien que ce cas soit d’origine traumatique, les fistules aorto-œsophagiennes peuvent aussi résulter de causes non traumatiques, comme la compression par un anévrisme aortique, des cancers gastro-intestinaux avancés, ou l’érosion de greffons aortiques dans le tractus digestif. Ces fistules sont potentiellement mortelles et se manifestent souvent par des hémorragies digestives, allant de saignements mineurs à des hémorragies massives avec défaillance hémodynamique. Les symptômes comprennent méléna, saignements visibles dans les selles ou hématémèse comme ici. Les fistules plus petites peuvent provoquer malaise ou ischémie des membres due à une réduction du débit sanguin. Le diagnostic est difficile et dépend de la stabilité du patient. Les patients stables sont explorés par endoscopie ou angio-CT, tandis que les patients instables nécessitent souvent une laparotomie urgente et des transfusions sanguines.
Ruptured Thoracic Aortic Aneurysm
Histoire clinique Aucune donnée clinique disponible pour ce spécimen.Pathologie Le cœur est présenté par sa face postérieure, montrant les deux ventricules. Une dilatation sacciforme importante de l’aorte thoracique ascendante est visible, avec plusieurs plaques athéromateuses. L’aorte est rompue en arrière, visible par une coloration foncée. Les deux ventricules sont hypertrophiés, les artères coronaires ainsi que les valves aortique et tricuspide sont normales. Il s’agit d’un anévrisme rompu de l’aorte ascendante. Informations complémentaires La dilatation de l’aorte ascendante est souvent une découverte fortuite lors d’une échocardiographie transthoracique. L’aorte thoracique se divise en trois parties : ascendante, crosse et descendante. L’aorte ascendante débute juste après la valve aortique et se termine avant la naissance du tronc brachiocéphalique, mesurant environ 5 cm. Elle comprend la racine aortique (avec les sinus coronaires et la jonction sinotubulaire) et la partie tubulaire ascendante. Plus de 50 % des anévrismes thoraciques se localisent ici, affectant la racine ou la partie tubulaire. Un anévrisme est une dilatation localisée de l’aorte supérieure de 50 % ou plus par rapport au diamètre attendu (rapport observé/attendu = 1,5), différent de l’ectasie qui est une dilatation diffuse inférieure à 50 %. L’incidence des anévrismes thoraciques ascendants est estimée à environ 10 pour 100 000 personnes-années. Référence : Saliba et al. (2015). Int J Cardiol Heart Vasc. 6: 91–100.
Calcified Aortic Valvular Stenosis Bicuspid Aortic Valve
Histoire cliniqueIl n'y a pas d’informations cliniques disponibles pour ce spécimen.Pathologie Ce spécimen est une coupe horizontale partielle de 1,5 cm à travers le plan de l’oreillette gauche. On y voit la surface interne lisse de l’oreillette, l’appendice auriculaire gauche et une partie du ventricule gauche. Sur la face supérieure, le tronc pulmonaire, une partie de la valve tricuspide pulmonaire, ainsi que l’aorte avec une valve aortique bicuspide anormale sont bien visibles. On observe des calcifications sur les bords opposés de cette valve ainsi qu’une autre calcification sur une cuspide pulmonaire. Informations complémentairesLa valve aortique bicuspide est l’anomalie cardiaque congénitale la plus fréquente, souvent non détectée avant l’âge adulte. Elle peut entraîner une sténose aortique plus ou moins sévère. Les symptômes peuvent inclure un souffle cardiaque, des douleurs thoraciques, une dyspnée, des palpitations et des signes d’insuffisance cardiaque tels que fatigue et œdème. Le rétrécissement oblige le ventricule gauche à fournir un effort accru, entraînant une hypertrophie, une dilatation et finalement une défaillance cardiaque. Des dépôts de calcium sur la valve, notamment chez les personnes présentant une valve bicuspide, conduisent à un raidissement des cuspides, ce qui aggrave la sténose.
Des répliques de corps humains pour améliorer l'enseignement !
La série révolutionnaire d'anatomie d'Erler- Zimmer comprend une collection unique et inégalée de répliques de corps humains colorées, spécialement conçues pour améliorer l'enseignement et l'apprentissage. Cette collection haut de gamme d'anatomie humaine extrêmement précise a été créée directement à partir de données radiologiques ou de préparations réelles à l'aide des dernières techniques d'imagerie. La série d'anatomie humaine 3D offre un moyen rentable de répondre à vos besoins spécifiques en matière d'enseignement et de démonstration dans l'ensemble du programme d'études de médecine, de sciences de la santé et de biologie. Une description détaillée de l'anatomie représentée dans chaque préparation imprimée en 3D est fournie. Quels sont les avantages de la série Anatomie 3D de Monash par rapport aux modèles en plastique ou aux véritables plastinats humains ?
Chaque réplique de corps a été soigneusement développée à partir de données radiologiques de patients ou de corps humains préparés de la plus haute qualité, sélectionnés par une équipe d'anatomistes hautement qualifiés au Centre d'enseignement de l'anatomie humaine de l'Université Monash, afin de représenter des zones cliniquement importantes de l'anatomie avec une qualité et un niveau de détail impossibles à obtenir avec des modèles conventionnels - il s'agit d'une véritable anatomie, pas d'une stylisation. Chaque réplique corporelle a été rigoureusement contrôlée par l'équipe d'anatomistes hautement qualifiés du Centre d'enseignement de l'anatomie humaine de l'Université de Monash, afin de garantir l'exactitude anatomique du produit final. Les répliques de corps ne sont pas de véritables tissus humains et ne sont donc soumises à aucune restriction en matière de transport, d'importation ou d'utilisation dans les établissements d'enseignement qui ne sont pas autorisés à utiliser des cadavres. Le site
série exclusive Anatomie 3D évite ces problèmes et d'autres problèmes éthiques qui surviennent lorsqu'on manipule des restes humains plastinés.